性質および化学反応
スコットランド南部の町ストロンチアンStrontianに産する毒重石によく似た鉱物ストロンチアン石は、バリウムおよびカルシウムとは明らかに異なる明るい赤色のスペクトルを示す元素を主成分とすることが見出され、この新発見の元素の名称の元となった。
銀白色の金属元素であるが空気中で酸化されやすく酸化ストロンチウムとなり、水とは速やかに反応して水素ガスを発生し水酸化ストロンチウムを生ずる。液体アンモニアに溶解し、青色の溶液を生ずる。明るい赤色の炎色反応を示す。
同位体のうち90Srはウランの核分裂生成物中に数%含まれ、体内に入るとストロンチウムはカルシウムと化学的性質が類似するために骨に蓄積し、放射線を出し続ける。1954年のビキニ環礁における核実験の際、マグロ漁船「第五福竜丸」は90Srを含む放射能灰を浴びる被爆事故に遭遇した。
| 大気中での酸化 |
2Sr + O2 → 2SrO |
ΔH °= -1184.0kJ |
| 水との反応 |
Sr + 2H2O → Sr(OH)2 + H2 |
ΔH °= -434.13kJ |
| ストロンチア水と二酸化炭素との反応 |
Sr(OH)2aq + CO2(g) → SrCO3(s)↓ + H2O |
Ksp = 5.6×10-10 |
| ストロンチウムイオンと硫酸イオンとの反応 |
Sr2+aq + SO42-aq → SrSO4(s)↓ |
Ksp = 3.4×10-7 |
| 90Srのβ-壊変 |
90Sr → 90Y + e- + 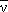 |
Q = +545.86keV |
 ストロンチウムの単体
ストロンチウムの単体
自然界における存在
性質の類似するカルシウム鉱物中に存在することがあるが、六方晶系の方解石中にはほとんど存在せず、斜方晶系の霰石中にカルシウムイオンを一部置換して存在する。独自の鉱物も形成し、ストロンチアン石SrCO3、天青石SrSO4およびスローソン石SrAl2Si2O8などがあり、バリウムと共存することが多い。
 |  |
| 天青石 マダガスカル産 | スローソン石 高知市円行寺産 |
工業的用途
明るい赤色の炎色反応を示すため、硝酸ストロンチウムは花火の着色および発火信号の火薬に用いられる。炭酸ストロンチウムはテレビのブラウン管用のガラスに添加され、放射線防除の役割を果たしている。フェライトSrFe2O4は最大エネルギー積が大きく、モーターおよび音響機器の磁性材料として用いられる。
主な化合物
化合物中ではストロンチウムは常に2価の陽イオンSr2+として存在する。
| SrO |
酸化ストロンチウム |
Strontium Oxide |
| Sr(OH)2·8H2O |
水酸化ストロンチウム八水和物 |
Strontium Hydroxide Octahydrate |
| SrCO3 |
炭酸ストロンチウム |
Strontium Carbonate |
| SrCl2·6H2O |
塩化ストロンチウム六水和物 |
Strontium Chloride Hexahydrate |
| SrSO4 |
硫酸ストロンチウム |
Strontium Sulfate |
| Sr(NO3)2·4H2O |
硝酸ストロンチウム四水和物 |
Strontium Nitrate Tetrahydrate |
|