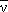性質および化学反応
カリウムKaliumはドイツ語であり、Potassiumとともに灰の意味を持つ。
銀白色の軟らかい金属元素であり性質はナトリウムに類似しているが反応性はより高い。空気中で極めて酸化されやすく過酸化カリウムK2O2を生成し、加熱により激しく燃焼し、超酸化カリウムKO2を生成する。水と反応してすぐに発火し淡紫色の炎を上げ水酸化カリウムとなり強いアルカリ性水溶液を生ずる。このため1族元素はアルカリ金属Alkaliと呼ばれる。化合物はイオン性が強く水溶性のものが多いが、過塩素酸塩KClO4 (Ksp = 1.05×10-2)およびヘキサクロロ白金酸塩K2[PtCl6] (Ksp = 7.5×10-6)など大きな陰イオンとの間に形成される化合物は難溶性であるものがある。
アルコールとも反応して溶解し、カリウムアルコキシドと水素を生成する。炎色反応は淡紫色であるが、不純物として少量でもナトリウムが混入していると黄色味を帯びた炎となる。
液体アンモニアに溶解し、青色の電導性溶液を生ずる。この溶液中にはカリウムイオンと溶媒和電子が存在し、濃厚溶液ではブロンズ様となり、液体金属に近い状態となる。
| 大気中での酸化 |
2K + O2 → K2O2 |
ΔH °= -494.1kJ |
| 大気中での燃焼 |
K + O2 → KO2 |
ΔH °= -284.93kJ |
| 水との反応 |
2K + 2H2O → 2KOH + H2 |
ΔH °= -393.09kJ |
| エタノールとの反応 |
2K + 2C2H5OH → 2C2H5OK + H2 |
| 液体アンモニアへの溶解 |
K + am → K+am + e-am |
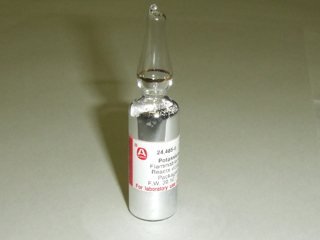 |  |
| カリウムの単体 | カリウムと水との反応 |
自然界における存在
カリウムは火成岩中に普遍的に存在する元素であり、地球内部よりも地殻上部に多く集中しているものと考えられる。これはマントルの主成分を構成していると考えられる、マグネシウムおよび鉄と比較してカリウムのイオン半径は極めて大きく、マントル中の岩石に取り込まれにくく、地球表層部の花崗岩に長石として濃縮されやすいからである。花崗岩中の主成分をなす正長石KAlSi3O8は、モースの硬度計で6度と定義される。また雲母K(Mg,Fe)3AlSi3O10(OH)2を構成する重要な元素でもある。海水中にもカリウムイオンとして溶存している。
天然放射性同位体である40Kは放射線エネルギーとしては弱いが、自然界での絶対存在量が多いためウランおよびトリウムと伴に天然放射能の約1/3を占める。
細胞内ではATPに貯蔵されたエネルギーを利用してカリウムイオンを細胞内に、ナトリウムイオンを細胞外に移動させるナトリウムポンプが働くことにより筋肉の運動が起こっている。このためカリウムイオンは生物にとって必須のミネラルである。
| 40K原子核の崩壊 |
40K + e- → 40Ar + ν
40K → 40Ca + e- + 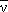 |
Q = +1504.69keV
Q = +1311.07keV |
 正長石 スペイン産
正長石 スペイン産
工業的用途
ナトリウムとの合金NaKは室温で液体であり、高速増殖炉などの冷却材に使用されている。石鹸は通常脂肪酸のナトリウム塩であるが、カリ石鹸の場合、溶解度が大きいため石鹸液などに用いられる。
カリウムは肥料の3要素の一つであり、植物のミネラルとして最も多く含まれる成分であるため、化学肥料として用いられる。
主な化合物
化合物中ではカリウムは常に1価の陽イオンK+として存在する。
| KOH |
水酸化カリウム(苛性カリ) |
Potassium Hydroxide |
| K2CO3 |
炭酸カリウム |
Potassium Carbonate |
| KCl |
塩化カリウム |
Potassium Chloride |
| K2SO4 |
硫酸カリウム |
Potassium Sulfate |
| KNO3 |
硝酸カリウム(硝石,焔硝) |
Potassium Nitrate |
|